Présentation
Auteur(s)
-
Théophile GUÉGUEN : Ingénieur Diplômé par l’État (DPE), Métallurgie Ancien Directeur technique à la Société Continentale Parker
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
La conversion chimique par phosphatation au zinc ou au zinc/fer des aciers ordinaires et des aciers faiblement alliés (teneur en éléments d’addition
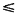 5 %) est couramment utilisée comme support de lubrifiants dans la déformation à froid (tréfilage, frappe à froid, étirage, extrusion).
5 %) est couramment utilisée comme support de lubrifiants dans la déformation à froid (tréfilage, frappe à froid, étirage, extrusion).
Les teneurs en éléments d’addition, tels que le Cr et le Mo, limitent les possibilités de la phosphatation, on constate qu’à partir d’une teneur en Cr de 2,5 à 3 %, les couches de phosphates ne présentent ni une adhérence, ni une homogénéité suffisantes, donc elles deviennent incompatibles avec des opérations de déformation à froid.
C’est alors que l’oxalatation offre une solution de rechange. Le développement de l’oxalatation fut en France très spectaculaire en particulier entre 1960 et 1970, dans le domaine de l’étirage de tubes et profilés et du tréfilage (substitut au plombage et au cuivrage).
DOI (Digital Object Identifier)
Cet article fait partie de l’offre
Traitements des métaux
(133 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Présentation
1. Principe du procédé
Après une préparation adaptée de la surface du métal, l’oxalatation en solution aqueuse est effectuée par immersion de 5 à 15 min, à une température de 50 à 65 C selon le type de bain (température la plus courante 60 à 65 C).
1.1 Constituants des bains
Acide oxalique : 30 à 60 g/L.
Activateurs : bifluorure (ou acide fluorhydrique), chlorure de sodium (ou acide chlorhydrique).
Accélérateurs de réaction : principalement thiosulfate ou thiocyanate.
Le pH des bains est de l’ordre de 1,6 à 1,7.
HAUT DE PAGE1.2 Réactions chimiques
Elles peuvent être résumées de la façon suivante :
-
réaction d’attaque du métal :
 ( 1 )
( 1 )
-
formation de la couche de conversion :
 ( 2 )
( 2 )
Les ions ferreux formés par la réaction [1] sont convertis en oxalate ferreux II [2] insoluble sous l’action des anions oxalate, et précipitent sur le métal du fait de l’élévation du pH à l’interface métal/solution. L’oxalate ferreux forme une couche très adhérente au métal ;
-
rôle de l’accélérateur, par exemple du thiosulfate de sodium (Na2 S2 O3) :

Les accélérateurs sont « consommateurs »...
Cet article fait partie de l’offre
Traitements des métaux
(133 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Principe du procédé
Cet article fait partie de l’offre
Traitements des métaux
(133 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive










