Présentation
Auteur(s)
-
Marcel CAUDE : Ingénieur du Conservatoire national des arts et métiers (CNAM) - Docteur ès sciences - Directeur de recherche au Centre national de la recherche scientifique (CNRS)
-
Didier THIÉBAUT : Docteur en pharmacie - Docteur de l’université Pierre et Marie Curie (Paris VI) - Chargé de recherche au CNRS
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
La chromatographie en phase supercritique, CPS (en anglais SFC : Supercritical Fluid Chromatography) met en œuvre, comme phase mobile, un fluide ou un mélange de fluides porté au-delà du point critique par un contrôle adéquat de la température et de la pression.
Cette technique est complémentaire des chromatographies en phases liquide et gazeuse (CPG). En effet, la CPG exige simultanément la volatilité et la stabilité thermique des solutés ; quant à la CPL, elle présente deux limitations :
-
l’obtention difficile de grandes efficacités ;
-
l’absence de détecteur aussi universel et sensible que le détecteur à ionisation de flamme (DIF) de la CPG.
Par suite, lorsqu’on est confronté à la séparation d’un mélange complexe de solutés non volatils, thermosensibles et non aisément détectables, ce qui représente environ 25 % des exemples rencontrés, on peut envisager de mettre en œuvre la CPS associée aux détecteurs de la CPG.
Enfin, la CPS possède des caractéristiques propres qui en font une technique chromatographique performante aussi bien avec des colonnes capillaires qu’avec des colonnes remplies :
-
de grandes efficacités par unité de temps peuvent être atteintes en raison de la diffusion rapide des solutés dans les fluides supercritiques du fait de leur faible viscosité ; aussi des séparations peuvent-elles être obtenues en des temps d’analyse 10 à 20 fois plus courts qu’en CPL ;
-
on peut aussi, pour la même raison, augmenter la longueur de la colonne, ce qui permet alors de disposer d’une très grande efficacité, même avec les colonnes remplies ;
-
des sélectivités importantes sont observées en raison des interactions entre les solutés, la phase stationnaire et la phase mobile que l’on peut faire varier par l’ajout de faibles quantités de modificateurs polaires à la phase supercritique ;
-
la CPS préparative présente l’avantage, par rapport à la CPL, d’une récupération rapide des solutés par détente de la phase mobile, en dépit des difficultés technologiques pour lesquelles diverses solutions ont été proposées.
VERSIONS
- Version archivée 1 de janv. 1992 par Marcel CAUDE, Didier THIÉBAUT
- Version archivée 3 de mars 2010 par Didier THIÉBAUT
- Version courante de sept. 2016 par Didier THIÉBAUT
DOI (Digital Object Identifier)
Cet article fait partie de l’offre
Techniques d'analyse
(290 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Des modules pratiques
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Présentation
1. Fluides supercritiques en chromatographie
1.1 Propriétés thermodynamiques
L’état thermodynamique d’un composé pur est déterminé par les trois variables pression P, volume V et température T. Il existe une relation entre ces trois variables, connue sous le nom d’équation d’état et représentée par une surface dans le référentiel à trois dimensions P, V, T. Tout corps pur, suivant la valeur des trois variables P, V, T sera sous la forme solide s, liquide
 , ou vapeur v. Les domaines d’existence de chacune de ces trois phases sont déterminés par l’équation d’état et peuvent être représentés sur plusieurs types de diagrammes : au diagramme tridimensionnel ( P, V, T ), on préfère généralement les projections sur les plans ( P, T ) (isochores) et (P, V ) (isothermes) d’une mise en œuvre plus aisée. Dans la majorité des cas, le volume V est remplacé par la masse volumique ρ, inversement proportionnelle à V. On utilise donc des diagrammes (P, ρ ) et (P, T ).
, ou vapeur v. Les domaines d’existence de chacune de ces trois phases sont déterminés par l’équation d’état et peuvent être représentés sur plusieurs types de diagrammes : au diagramme tridimensionnel ( P, V, T ), on préfère généralement les projections sur les plans ( P, T ) (isochores) et (P, V ) (isothermes) d’une mise en œuvre plus aisée. Dans la majorité des cas, le volume V est remplacé par la masse volumique ρ, inversement proportionnelle à V. On utilise donc des diagrammes (P, ρ ) et (P, T ).
Le diagramme (P, T ) (figure 1) précise les domaines des trois états de la matière, s,
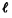 , v. Les raccordements de ces différents domaines correspondent aux transitions de phase, s’accompagnent de discontinuité de certaines propriétés physiques, ρ en particulier, et correspondent aux équilibres liquide-vapeur
, v. Les raccordements de ces différents domaines correspondent aux transitions de phase, s’accompagnent de discontinuité de certaines propriétés physiques, ρ en particulier, et correspondent aux équilibres liquide-vapeur
 , solide-liquide
, solide-liquide
 et solide-vapeur ( s-v). Au point triple T coexistent les trois phases solide-liquide-vapeur.
et solide-vapeur ( s-v). Au point triple T coexistent les trois phases solide-liquide-vapeur.
On...
Cet article fait partie de l’offre
Techniques d'analyse
(290 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Des modules pratiques
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Fluides supercritiques en chromatographie
Cet article fait partie de l’offre
Techniques d'analyse
(290 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Des modules pratiques
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive










