Présentation
Auteur(s)
-
Émile KUNTZ : Ingénieur chimiste de l’École supérieure de chimie industrielle de Lyon - Licencié en sciences économiques de l’université de Lyon Laboratoire de chimie organométallique de surface (CPE Lyon)
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
L’hydroformylation (ou synthèse oxo) consiste à faire réagir un composé oléfinique avec un mélange d’oxyde de carbone et d’hydrogène sous pression pour former un aldéhyde selon la réaction :
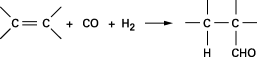
Les deux métaux les plus efficaces pour catalyser cette réaction sont le cobalt et le rhodium. Les formes actives de ces deux métaux sous formes d’hydrures carbonylés sont solubles dans le milieu réactionnel, ce qui confère à l’hydroformylation le caractère d’une réaction catalytique homogène.
À partir, principalement, des oléfines linéaires terminales, les aldéhydes obtenus sont des produits de chimie de base importants qui peuvent être convertis en alcools, esters, acides, amines, etc.
L’hydroformylation du propène en butanal (et en isobutanal), qui permet d’accéder au butanol, à l’isobutanol et au 2-éthylhexanol, représente 70 % des capacités mondiales d’hydroformylation (tableau 1).
Les alcools courts (C3 à C5) et leurs esters sont utilisés principalement comme solvants tandis que les alcools à longue chaîne (C12 à C18) sont utilisés pour la production de détergents. Les phtalates d’alcoyles (C8 à C10) sont employés comme plastifiants, notamment du PVC.
Depuis 1974, la plupart des unités de production d’aldéhydes (C3, C4, C5) par catalyse au cobalt ont été remplacées par des unités opérant dans des conditions plus douces, à plus basse pression, en présence de catalyseurs au rhodium. Le rendement en aldéhydes est supérieur à 95 % et même 99 % pour certains procédés. L’utilisation du rhodium en catalyse homogène est complètement maîtrisée dans le réacteur et dans les opérations de recyclage et de régénération. En particulier, le procédé Ruhrchemie-Rhône-Poulenc, qui utilise un système biphasique avec séparation du catalyseur par décantation, a permis une grande simplification du procédé d’hydroformylation du propène et du butène. Avec le rhodium, le même concept de séparation du catalyseur par décantation a permis l’industrialisation de la synthèse du butanediol par hydroformylation de l’alcool allylique, du nonanediol par hydroformylation de l’oct-7-én-1-al et de divers intermédiaires. Toutefois la catalyse au cobalt demeure très compétitive dans la production des alcools utilisés pour la fabrication des détergents.
De nombreuses innovations ont provoqué un regain en recherche industrielle et universitaire depuis 1995 (250 publications ou brevets par an).
Ces améliorations ont conforté la position de la réaction d’hydroformylation pour la production d’alcools primaires et de leurs dérivés à partir des alcènes (ou oléfines). Les efforts déployés en recherche depuis 1980 pour améliorer les performances des réactions d’oxydation des alcanes, d’hydratation des oléfines et du butadiène, n’ont pas obtenu des résultats permettant de concurrencer la réaction d’hydroformylation.
VERSIONS
- Version archivée 1 de juin 1986 par Hans LEMKE
DOI (Digital Object Identifier)
Cet article fait partie de l’offre
Opérations unitaires. Génie de la réaction chimique
(370 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Des modules pratiques
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Présentation
1. Réaction chimique et catalyseurs d’hydroformylation
1.1 Réaction chimique
L’hydroformylation a été découverte en 1938 par Roelen de Ruhrchemie qui mit en évidence la formation de propanal à partir d’éthylène, de CO et de H2, à température et pression élevées, en présence de catalyseur au cobalt [1]. L’hydroformylation peut être appliquée à un grand nombre d’alcènes à chaîne linéaire ou ramifiée, à double liaison interne ou terminale. La réaction a lieu à des températures et des pressions élevées avec le cobalt (entre 100 et 200 ˚C et 100 et 300 bar) et inférieures avec le rhodium (entre 50 et 130 ˚C et 5 et 50 bar).
La réaction sur une oléfine terminale donne naissance à deux aldéhydes : l’isomère linéaire (n) et l’isomère ramifié (iso). La sélectivité d’un catalyseur en produit linéaire (n/n+iso) est un paramètre important. Ainsi, l’heptanal(n) et le 2-méthylhexanal (iso) sont obtenus avec l’hex-1-ène suivant la réaction :

Les réactions secondaires constatées sont les suivantes (figure 1) :
-
hydrogénation de l’oléfine en alcane (figure 1 a) ;
-
isomérisation de l’oléfine (oléfine à double liaison terminale en oléfine à double liaison interne) (figure 1 b) ;
-
formation de cétones (figure 1 c) ;
-
réduction de l’eau par l’oxyde de carbone avec formation d’hydrogène et de gaz carbonique (figure 1 d).
Les réactions secondaires mettant en œuvre les aldéhydes formés sont beaucoup plus importantes. L’aldéhyde peut être hydrogéné en alcool ou transformé en acide en présence de traces d’oxygène....
Cet article fait partie de l’offre
Opérations unitaires. Génie de la réaction chimique
(370 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Des modules pratiques
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Réaction chimique et catalyseurs d’hydroformylation
ANNEXES
Quelques renseignements concernant les capacités de production sont donnés tableaux 1 et 2. Des compléments actualisés peuvent être trouvés dans les références et .
HAUT DE PAGERéférences
ROELEN (O.) - * - Ruhrchemie AG. BF 860 289 (1939).
BROUGHTON (D.B), BERG (K.) - * - Hydrocarb. Process 48 (6) p. 115 (1969).
ZIEGLER (K.) - * - Chimie et Industrie 92 p. 631 (1964).
SHERWOOD (P.W.) - * - Chimie et Industrie 85 p. 576 (1961).
CHAUVIN (Y.) - * - Chem. Ind. (GB) p. 376 (1974).
OTTON (J.) - * - Information Chimie (F) 161 p. 161 (mai 1980).
WEISSERMEL (K.), ARPE (H.J.) - Synthèses à base d’oxyde de carbone - . Dans : Chimie Organique Industrielle p. 113-126 Masson S.A. (1981).
CORNILS (B.), WIEBUS (E.) - * - Journal of the Royal Netherlands Chem. Soc. 115 p. 211-215 (1996).
KUNTZ (E.) - * - Chemtech 17 p. 570-575 (1987).
FROHNING (C.D.), KOHLPAINTER (W.) - Hydroformylation - . Dans : Applied Homogeneous Catalysis with Organometallic Compounds, vol. no 1 p. 29-104 VCH (1996).
CORNILS (B.) - Oxo synthesis. Roelen reaction - . Dans : New Synthesis with Carbon Monoxide, p. 1-225 Verlag S. (1980).
LEMKE (H.) - * - Génie Chimique 89 p. 118 (1963).
LEMKE (H.) - * - Hydrocarb. Process 45 (2) p. 148 (1966).
WILKINSON (G.) - * - Brit. Pat. 1 138 601 (1964).
EVANS (G.), OSBORN (J.A.), WILKINSON (G.) - * - J. Chem. Soc(A) p. 3133 (1968).
PRUETT (R.L.) - * - Union...
Cet article fait partie de l’offre
Opérations unitaires. Génie de la réaction chimique
(370 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Des modules pratiques
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive










