Des chercheurs de l'Imperial College de Londres et du laboratoire Chimie de la matière condensée de Paris ont conçu et élaboré des nanoparticules hybrides d'or et de silice, qui se révèlent être de véritables « couteaux-suisses » thérapeutiques.
Testées sur des cellules humaines en culture et chez la souris, elles permettent de combiner deux modes de traitement des tumeurs et trois techniques d’imagerie. Elles auraient notamment une capacité de stockage et de transport des médicaments plus importante que les vecteurs actuellement sur le marché, ce qui augure de perspectives intéressantes en cancérologie. Ces résultats sont publiés dans la revue PNAS, le 4 février 2015.
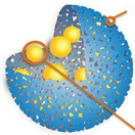
Concevoir un outil permettant de coupler trois techniques d’imagerie complémentaires (IRM, imagerie par fluorescence et un type d’imagerie ultrasonore dite « photo-acoustique ») et deux types de traitements (chimiothérapie et thérapie photo-thermique), le tout dans une sphère de 150 nanomètres de diamètre, c’est la prouesse que vient de réussir une équipe internationale de chimistes et de spécialistes d’ingénierie biomédicale. Pour cela, les chercheurs ont synthétisé des objets hybrides, constitués d’une coque de silice nanoporeuse abritant des nanoparticules d’or aux propriétés exceptionnelles : les clusters d’or.
Les clusters d’or sont des nanoparticules de petite taille (moins de 2 nanomètres) possédant des propriétés intéressantes (fluorescence, production de chaleur, magnétisme), très différentes de celles de l’or massif ou même des nanoparticules d’or plus grosses. Toutefois, leur manque de stabilité en milieu aqueux (elles ont tendance à s’agréger pour former des particules plus grosses) a jusqu’à présent empêché leur utilisation en biologie et médecine. En faisant « infuser » des coques en silice poreuses avec des précurseurs d’or, les chercheurs ont réussi à former des clusters d’or dans les pores de l’enveloppe (ce qui les stabilise) et des nanoparticules d’or plus grosses dans la cavité centrale. Cette structure de « hochet quantique » est stable en solution aqueuse, pénètre au cœur des cellules sans toxicité, et préserve les propriétés optiques et magnétiques des clusters d’or, tout en permettant de maximiser leur capacité de stockage de médicament.

L’incorporation d’or, hydrophobe, dans la sphère de silice a permis d’accroître très significativement les capacités de stockage de doxorubicine, un agent anticancéreux souvent difficile à stabiliser dans ce genre de matrice poreuse. Les chercheurs estiment que, par rapport aux vecteurs actuellement commercialisés (de type liposome), la proportion des molécules qui atteindraient leur cible passerait de 5 % à 95 %. A cette capacité de transport de médicaments s’ajoute un potentiel en thérapie photo-thermique : en effet, lorsqu’elles sont activées par un laser infrarouge, les particules contenant des clusters d’or émettent une fluorescence infrarouge, mais aussi suffisamment de chaleur pour tuer les cellules cancéreuses : leur température s’élève ainsi jusqu’à 51°C, ce qui cause leur mort. Chez la souris, cela a permis de réduire de 55 % la masse tumorale après un seul traitement.
Cette production de chaleur peut être exploitée aussi dans un objectif d’imagerie : elle provoque une dilatation transitoire des clusters d’or, ce qui produit des ultrasons, détectables comme lors d’une échographie. Par ailleurs, la fluorescence émise par les particules stimulées au laser traverse les tissus (qui n’absorbent pas les infrarouges de cette longueur d’onde) : elle peut donc être mesurée de manière non invasive. Enfin, pour des tailles inférieures à 2 nanomètres, l’or devient magnétique. Il est donc possible d’utiliser les hochets quantiques comme agent de contraste pour l’imagerie par résonance magnétique (IRM). Ces trois méthodes d’imagerie (imagerie par fluorescence infrarouge, imagerie photo-acoustique et IRM) permettent d’observer la tumeur de manière complémentaire, avec au final de très bonnes résolutions spatiale et temporelle.
Les scientifiques cherchent maintenant à optimiser ces nano-vecteurs. Ils aimeraient « fonctionnaliser » leur surface avec des marqueurs, afin qu’ils reconnaissent et ciblent spécifiquement les cellules cancéreuses. Enfin, ils espèrent parvenir à réduire la taille des particules d’or présentes dans la cavité centrale pour rendre le vecteur complètement biodégradable.
Source : CNRS




















Réagissez à cet article
Vous avez déjà un compte ? Connectez-vous et retrouvez plus tard tous vos commentaires dans votre espace personnel.
Inscrivez-vous !
Vous n'avez pas encore de compte ?
CRÉER UN COMPTE